Entwicklung und Zulassung von Impfstoffen
Wie alle Arzneimittel werden Impfstoffe gemäß aktuellen behördlichen Richtlinien und gesetzlichen Anforderungen und unter Berücksichtigung wissenschaftlicher Leitlinien entwickelt, geprüft und zugelassen. Ziel ist die Bereitstellung eines qualitativ hochwertigen, wirksamen und vor allem sicheren Impfstoffs.
Die Dauer von der Idee bis zum zugelassenen Impfstoff hängt von vielen Variablen ab. Handelt es sich um eine bekannte oder neue Herstellungstechnologie(„Plattform“), ist es ein weiterer altbekannter Impfstoff (z.B. gegen Keuchhusten) oder eine Innovation, geht es um einen Kombinations-Impfstoff mit unterschiedlichen Wirkstoffen (Antigenen) oder um eine bekannte oder neuartige Applikationstechnik. Neben sehr speziellem Know-how für diese komplexen Arzneimittel, die zu den „Biologika“ zählen, sind auch enorme finanzielle Mittel und ein langer Atem gefragt, denn nur ein Bruchteil aller geprüften Substanzen schafft es bis zur Marktreife.
Und selbst wenn man das hier skizzierte vollständige Entwicklungsprogramm bis zur Zulassung erfolgreich durchlaufen hat, gilt es noch die große Herausforderung der behördlichen Zulassung zu bestehen. Ist dies gelungen, erfolgt die Produktion im „großen Maßstab“ für den Markt.
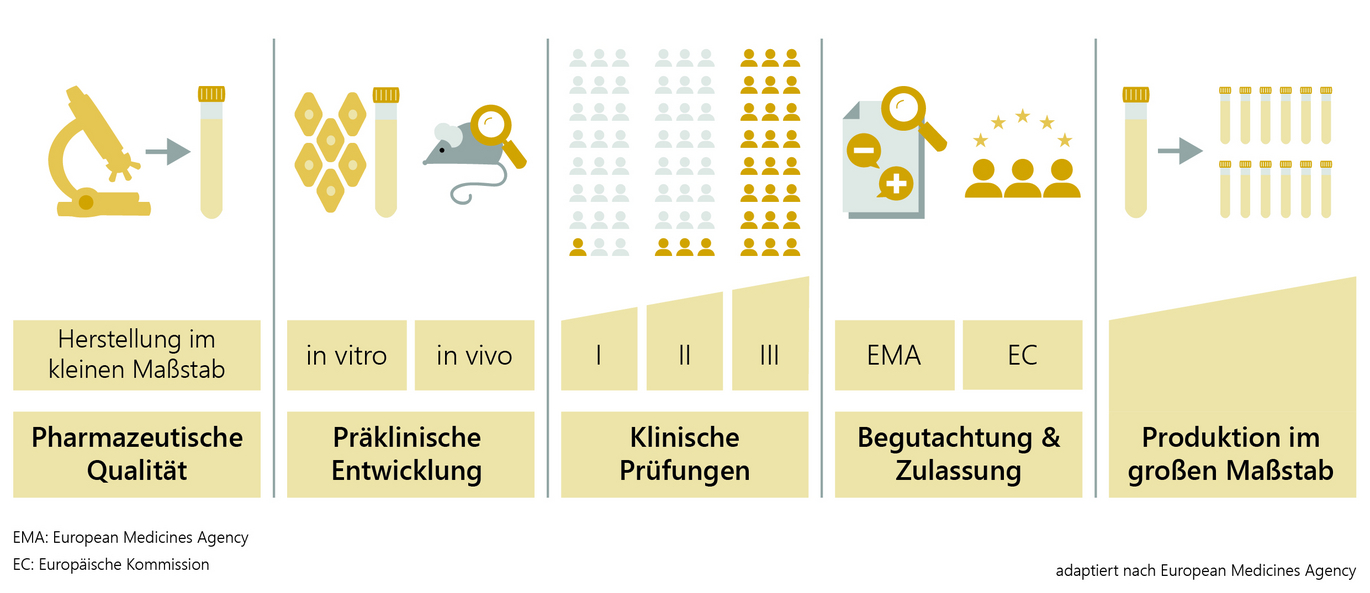
Entwicklung von Impfstoffen
Die Identifikation und Erforschung eines Impfstoffkandidaten im Labor dauert etwa zwei bis fünf Jahre. Zunächst wird der Krankheitserreger (Virus oder Bakterium) analysiert und geprüft, welche Bestandteile sich am besten eignen, damit das Immunsystem des Menschen reagieren und einen ausreichenden Schutz (z.B. Antikörper) aufbauen kann. Danach folgen die Entwicklung des Impfstoffs und die Herstellung im kleinen Maßstab für die weitere Impfstoffprüfung an Tier (Präklinik) und Mensch (Klinik).
In der präklinischen Impfstoffentwicklung werden in Zellkulturen (in vitro, z.B. mit Immunzellen des Menschen) und in Tierversuchen (in vivo) Immunogenität (Fähigkeit des Antigens, eine Immunisierung auszulösen), Wirksamkeit und Sicherheit des Impfstoffs getestet. Auch das nimmt etwa zwei bis fünf Jahre in Anspruch.
Erst nach umfangreichen Untersuchungen und dem Nachweis, dass der Impfstoff in guter Qualität und allen hohen Anforderungen entsprechend hergestellt werden kann, wird der Impfstoff in klinischen Prüfungen an freiwilligen und über alle eventuellen Risiken aufgeklärten Studienteilnehmerinnen und Studienteilnehmern erprobt:
Klinische Prüfungen
Die zuständigen nationalen Behörden und Ethikkommissionen stellen sicher, dass alle Studien wissenschaftlich gesichert und ethisch korrekt durchgeführt werden. Klinische Studien vor der Impfstoffzulassung lassen sich in drei Phasen einteilen.
Phase I: In der Regel sind zwischen 20 und 100 gesunde freiwillige Probandinnen und Probanden beteiligt, um anhand von Labortests zu prüfen, ob der Impfstoff die erwarteten Reaktionen auslöst (Immunogenität). In erster Linie wird hier aber die Sicherheit und Verträglichkeit getestet.
Phase II: Untersuchungen an mehreren hundert freiwilligen Probandinnen und Probanden geben Aufschluss über die bestmögliche Impfstoffdosierung für einen optimalen Schutz, das Nebenwirkungsprofil und die Anzahl der benötigten Impfungen für ein bestmögliches Impfschema.
Phase III: In der letzten Phase wird der Impfstoff an einigen tausend (im Falle der ersten COVID-19-Impfstoffe an mehreren 10.000en) freiwilligen Probandinnen und Probanden in der Zielpopulation getestet. Hier muss gezeigt werden, wie wirksam der Impfstoff im Vergleich zu einer Kontrollgruppe (z. B. Placebo) gegen die Erkrankung schützt und welche Nebenwirkungen mit welcher Häufigkeit gegebenenfalls auftreten können.
Die Zulassung
Ein behördliches Zulassungsverfahren ist grundsätzlich Voraussetzung dafür, dass ein Impfstoff auf den Markt kommt. Zulassung bedeutet: Prüfung eines Impfstoffs auf Qualität, Wirksamkeit und Sicherheit auf Basis der von der Antragstellerin oder vom Antragsteller vorgelegten Daten.
Antragsteller und auch das Gesetz legen fest, ob ein Impfstoff nur in einem Land (national), in mehreren europäischen Ländern oder im Zuge des sog. „Zentralen Verfahrens“ im gesamten EWR Raum (EU-Länder und Norwegen, Island und Liechtenstein) zur Zulassung eingereicht werden kann.
Die Antragstellerin oder der Antragsteller reicht Zulassungsunterlagen nach klar vorgegebenen Richtlinien zur behördlichen Begutachtung ein. Diese beinhalten u.a. regulatorische Angaben, Daten zur Herstellung, präklinische und klinische Daten, aktuelle Fachliteratur sowie Informationen zur geplanten langfristigen Überwachung nach erfolgter Zulassung. Neben dem Impfstoffantigen, dem „eigentlichen Wirkstoff“, werden auch sämtliche anderen Inhaltsstoffe eines Impfstoffs bewertet. Das Europäische Arzneibuch, das Gesetzescharakter hat, definiert diese Inhaltsstoffe inklusive ihrer zulässigen Grenzwerte. Zusätzlich gilt es eine Unzahl an vorgeschriebenen Gesetzen und regulatorisch-wissenschaftlichen Regelwerken zu beachten.
Arzneimittelbehörden nehmen nach Begutachtung all dieser Daten und Studien, die im Zuge des Entwicklungsprogramms erhoben und durchgeführt wurden, final die Bewertung des sich daraus ergebenden Nutzen-Risiko-Profils vor.
In der EU wird das sog. „Zentrale Zulassungsverfahren“ für viele Impfstoffe wie auch für alle COVID-19-Impfstoffe durch die Europäische Arzneimittelagentur (European Medicines Agency - EMA) in Amsterdam koordiniert. Bei der fachlichen Begutachtung sind die nationalen Arzneimittelbehörden der EU sowie von Norwegen, Island und Liechtenstein eingebunden.
Erfüllt der Impfstoff alle wissenschaftlich-regulatorischen Voraussetzungen und überwiegt sein Nutzen gegenüber etwaigen Risiken, wird nach erfolgreichem Zulassungsverfahren vom CHMP, dem Expertinnen- und Expertengremium der EMA (bestehend aus Fachexpert:innen der EWR-Mitgliedsländer, Patientenvertreter:innen u.W.) eine Zulassungsempfehlung für den Impfstoff an die Europäische Kommission abgegeben, die die Zulassung erteilt. Eine nationale Zulassung ist nicht mehr erforderlich. Ein Zulassungsverfahren kann bis zu zwei Jahre dauern.
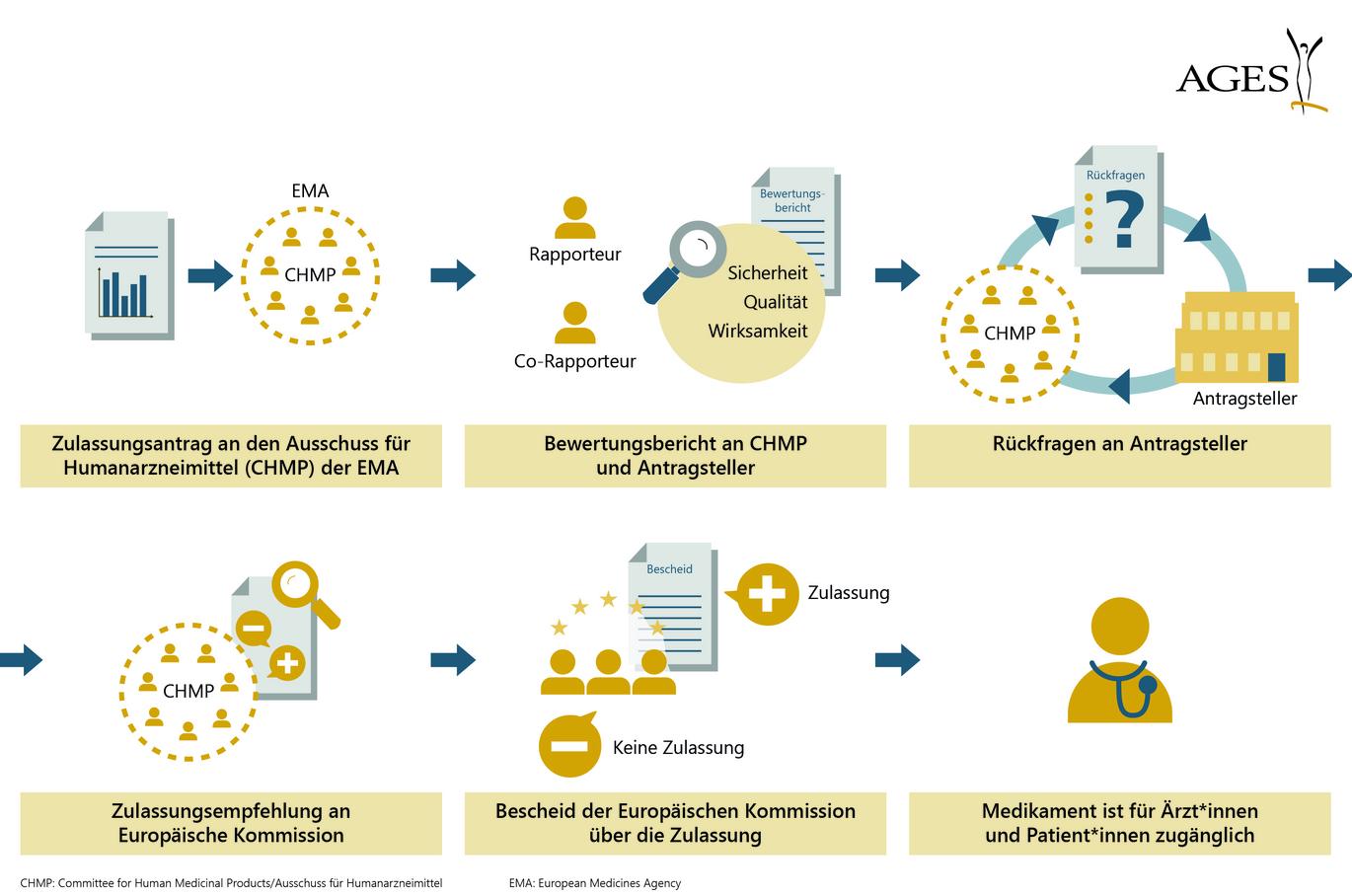
Zusätzlich ist in Österreich eine Chargenfreigabe durch ein behördlich ernanntes Arzneimittelkontrolllabor notwendig (OMCL – Official Medicines Control Laboratory der AGES), bevor der Impfstoff auf den Markt kommen darf. Eine Charge ist eine im Zuge eines einheitlichen Herstellungsvorgangs produzierte Menge eines Impfstoffs. Jedes Arzneimittelkontrolllabor in der EU bzw. im Europäischen Wirtschaftsraum (EWR) und in der Schweiz kann, wenn es die gesetzlichen Anforderungen erfüllt, eine Chargenfreigabe für Impfstoffe durchführen. Die Freigabezertifikate müssen dann in der ganzen EU bzw. im ganzen EWR und in der Schweiz anerkannt werden. Die Herstellerinnen und Hersteller können selbst entscheiden, bei welchem Arzneimittelkontrolllabor sie ihren Impfstoff für eine Chargenfreigabe einreichen.
COVID-Impfstoffe
Die Entwicklung und der Zulassungsprozess von COVID-19-Impfstoffen verliefen anfangs aufgrund der schwerwiegenden Folgen dieser Pandemie ohne verfügbare, zugelassene Covid-Impfstoffe in beschleunigter Form. Dabei floss umfassendes bereits vorhandenes Wissen über Coronaviren und Impfstoffentwicklung ein.
Um die Entwicklung zu beschleunigen, setzten Unternehmen und Forschungseinrichtungen wesentlich mehr Personal und finanzielle Ressourcen in kürzerer Zeit ein als bei herkömmlichen Entwicklungsprozessen. Wo dies unter Einhaltung der strengen Sicherheitsauflagen möglich war, wurden auch Studienphasen parallel statt wie sonst üblich hintereinander durchgeführt. Darüber hinaus erweiterten Herstellerinnen und Hersteller ihre Produktionsanlagen zu einem wesentlich früheren Zeitpunkt der Impfstoffentwicklung als üblich, damit nach Zulassung binnen kürzester Zeit rasch große Impfstoffmengen verfügbar sind.
Seitens EMA und Europäischen Arzneimittelbehörden wurden in dieser Zeit ebenfalls alle Kräfte vereint, um rasch einen qualitativ hochwertigen, wirksamen und sicheren Impfstoff der Europäischen Bevölkerung zur Verfügung zu stellen, was auch gelang. Diese Impfstoffe hatten einen immensen Beitrag geleistet, schweren Komplikationen mit Krankenhausaufenthalten und Todesfällen vorzubeugen.
Schon längst laufen Zulassungen für COVID-19-Impfstoffe nicht mehr forciert ab, da ausreichend zugelassene Impfstoffe zur Verfügung stehen. Sie werden genauso zugelassen, wie jeder andere Standard-Impfstoff auch.
Impfstoffsicherheit nach der Zulassung
Impfstoffe werden nicht nur vor und während der Zulassung, sondern auch solange sie auf dem Markt sind, kontinuierlich überwacht. Unter Pharmakovigilanz wird dabei eine Vielzahl von Methoden und Aktivitäten verstanden, die es u.a. ermöglichen sollen, Nebenwirkungen zu detektieren, zu bewerten, zu verstehen und weiteren vorzubeugen.
Teil der Pharmakovigilanz ist die Meldepflicht von Angehörigen der Gesundheitsberufe im Zusammenhang mit der Anwendung von Impfstoffen. Sie besteht bei Humanarzneimitteln für vermutete Nebenwirkungen und auch für das Ausbleiben der erwarteten Wirksamkeit. Aber nicht nur Mitarbeiterinnen und Mitarbeiter im Gesundheitswesen, sondern auch Patientinnen und Patienten und deren Angehörige können vermutete Nebenwirkungen melden. Meldungen sind elektronisch oder schriftlich an das Bundesamt für Sicherheit im Gesundheitswesen (BASG) zu übermitteln.
Sämtliche Meldungen vermuteter Nebenwirkungen werden EU-weit gesammelt. Die Analyse all dieser Daten ermöglicht es, auf nationaler und europäischer Ebene ein mögliches neues Risiko zu erkennen (Signaldetektion), genau zu prüfen und damit zu mehr Arzneimittelsicherheit für alle Patientinnen und Patienten beizutragen. Wird ein Signal detektiert, wird dieses im europäischen Kontext im sogenannten PRAC (Pharmacovigilance Risk Assessment Committee) der EMA bewertet. Je nach Ergebnis der Bewertung werden Maßnahmen wie die Aufnahme von neuen Warnhinweisen in der Fach- bzw. Gebrauchsinformation oder im Extremfall sogar die Aufhebung der Zulassung eines Impfstoffs ergriffen.
Als weitere Sicherheitsmaßnahmen erfolgt für jede neue Charge weiterhin eine verpflichtende Chargenprüfung durch ein OMCL. Nur nach zertifizierter Chargenfreigabe kann ein Impfstoff dem Gesundheitspersonal und letztlich dem Impfling zur Verfügung stehen.
Impfstoff Informationen
Weitere Informationen zu Arzneimitteln, Impfstoffen und Medizinprodukten sowie zur Zulassung finden Sie auf den Websiten des Bundesamts für Sicherheit im Gesundheitswesen (BASG), des Bundesministeriums für Arbeit, Soziales, Gesundheit, Pflege und Konsumentenschutz (BMASGPK) bzw. der Europäischen Arzneimittelagentur (EMA):
Aktualisiert: 27.05.2026